Structure chimique des colorants
Un article de Les colorants alimentaires.
| Sommaire [cacher] |
Nature chimique des colorants
Les colorants ont véritablement un pouvoir pour donner une certaine couleur à un produit. Cette théorie a été proposée par O. N. Witt en 1876, lors du grand essor des recherches sur les colorants de synthèse. Le groupe d'atomes responsable de la coloration du composé s'appelle le chromophore. Il doit être associé à un auxochrome afin de fixer les "molécules colorées" sur le produit, le substrat.
Les chromophores
Le groupe chromophore est le groupe qui donne la couleur du colorant, et il est donc contenu dans tous les colorants.
Il est donc possible de classer les colorants suivant leur groupe chromophore :
Il peut s'agir de dérivés :
- éthyléniques avec un ou plusieurs groupes (-C=C- ou CH3-CH2)
- carbonylés (-C=O)
- nitrosés (-N=O)
- nitrés à base de 
- azoïques (-N=N-)
L'influence des atomes chromophores est d'ailleurs renforcée si ceux-ci sont sous forme d'ions.
On peut aussi les classer suivant leur mode de synthèse :
- les nitrosés, synthétisés par une transformation chimique mettant en jeu de l'acide nitreux (HNO2) et qui donnent des laques
- les nitrés, formés dans des transformations chimiques ayant en parti comme réactif l'acide nitrique (HNO3 ⇒ H+ + NO3-), et de couleur jaune ou orangée
-les stilbéniques, qui dérivent du stilbène (C6H5-CH=CH-C6H5), également de teinte jaune ou orangée
Les auxochromes
Les groupes auxochromes, qui permettent la fixation des colorants sur les substrats, sont essentiellement :
- des groupes acides (-COOH, -SO3H, -OH,...), qui permettent aussi une meilleure solubilité dans l'eau
- des groupes basiques (surtout du -NH2 et SO3- parfois)
Pour fixer les atomes chromophores sur le "substrat", les auxochromes peuvent par exemple utiliser leur forme polaire, c'est-à-dire d'ion. En effet, ils utilisent leur électronégativité pour créer des liaisons ioniques qui fixent le colorant sur le substrat. Souvent, les groupes auxochromes sont composés d'un noyau quinoïde, un cycle de 6 atomes de carbone reliés entre eux par 4 liasons simples et 2 liaisons doubles
La deuxième propriété importante des groupes auxochromes est "d'amplifier la couleur", c'est à dire d'élargir les bandes d'absorption. Il peut le faire vers les petites longueurs d'ondes (effet hypsochrome) ou vers les grandes (effet bathochrome).
Exemple (Formules topologiques)
Azoïque
Tartazine (E102; couleur jaune):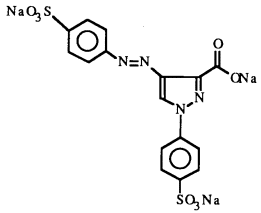
Il est azoïque car il possède une double liaison azote en son centre.
Ethylénique
Bleu Patenté V (E131, couleur bleu)

Ce colorant est un éthylénique car les segments seuls sont en fait des liaisons carbone-carbone, et les trois parties de la molécules sont reliées par ces liaisons. De plus, il dispose de C2H5, qui sont en fait des groupes éthyles CH3-CH2
Page suivante : Utilisation et nature des colorants
Retour à la page Les colorants et le goût
Retour à la page d'Accueil
